行业创新者面临的市场准入挑战
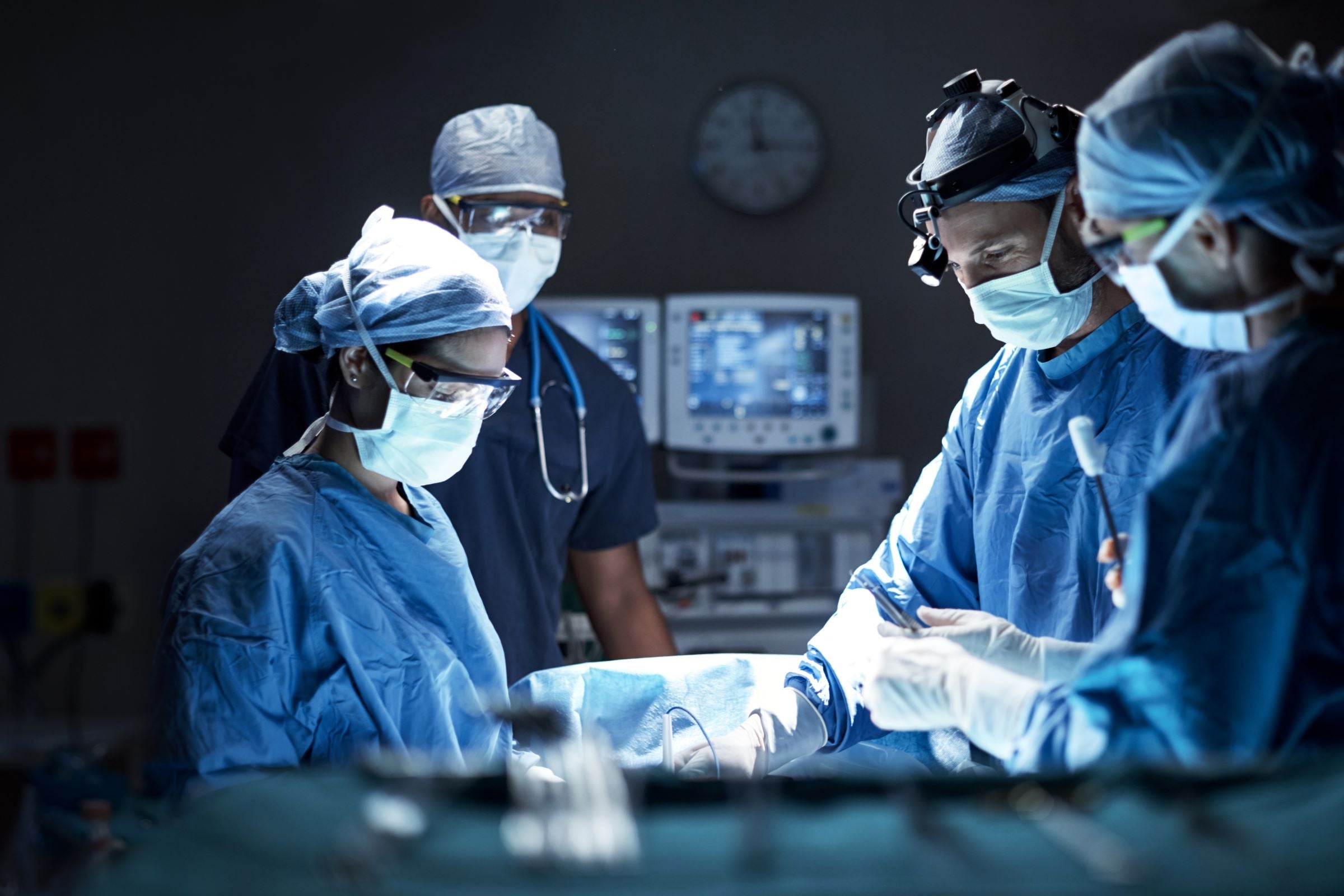
随着医疗器械互操作性的增强以及数字健康技术的蓬勃发展,医疗器械的安全性、性能和质量标准正在发生转变。这些趋势扩大了合规与风险管理的范围,使健康与生命科学企业的市场准入面临更大挑战。采用既能支持快速创新,又能满足可用性、安全性及全球法规与标准的产品开发流程至关重要*。
数字健康技术的普及

以用户为中心的产品开发存在专业知识缺口

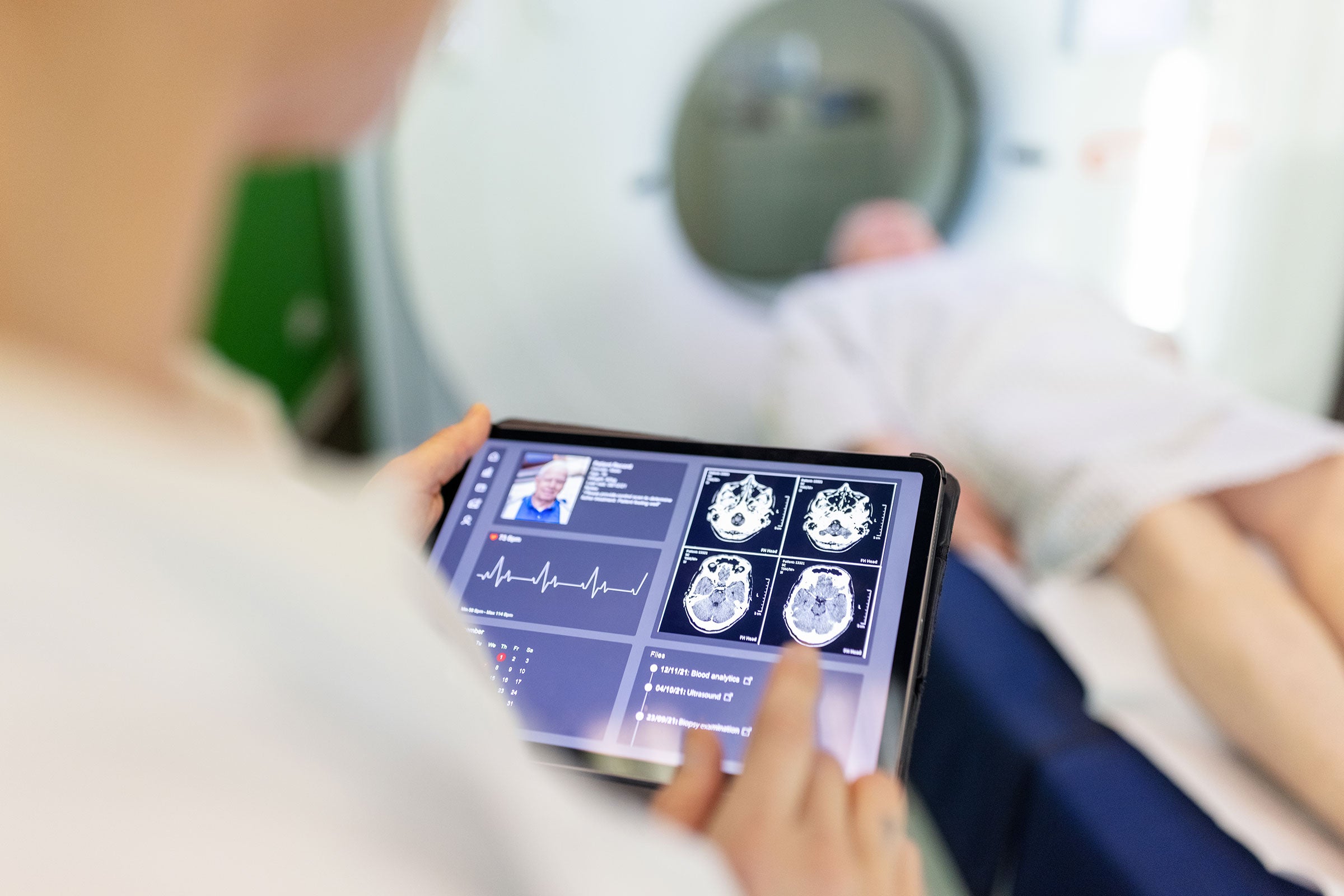
复杂的监管环境
35%
的美国成年人每天至少使用一次可穿戴医疗设备。(信息来源)
14%
2024 年医疗设备召回增幅(受更严格的监管和执法推动)。(信息来源)
17.7 亿
预计到 2029 年,将有 17.7 亿人开始使用数字健康产品。(信息来源)
34%
的医疗产品因设计控制不当而被召回。(信息来源)
我们助力行业创新者自信地进入高度监管的市场


弥补产品开发专业知识差距
借助人因工程 (HFE) 咨询与软件*,实现合规的产品开发。
证明安全性并验证性能
通过我们严格的测试和认证,符合市场标准、法规及最佳实践。

自动化处理并简化法规事务
借助全球法规专业知识和软件*,简化医疗市场准入流程。
满足产品可用性、安全性与法规要求
健康与生命科学领域的测试和认证
赋能健康与生命科学行业创新者,支持安全、合规与可持续发展
我们的安全科学专业知识与软件解决方案,助力行业创新者加速市场准入流程、管理网络安全风险、构建合规员工队伍、加强供应商风险管理并增强 ESG 管理能力,助其开发更安全合规的医疗产品与系统。
认识我们的专家


面向健康与生命科学行业的综合性解决方案
* UL Solutions 为医疗器械行业提供广泛的服务方案,包括认证、批准/公告机构及咨询服务。为了防止利益冲突(或疑似利益冲突),以及维护我们自身及客户的品牌声誉,我们已建立标准化流程以识别、管理潜在利益冲突并确保公正性。UL Solutions 无法向欧盟 MDD(《医疗器械指令》)、MDR(《医疗器械法规》)、IVDD(《体外诊断医疗器械指令》)或 IVDR(《体外诊断医疗器械法规》)公告机构、UKCA MD(英国合格评定医疗器械)认证机构或 MDSAP(医疗器械单一审核程序)客户提供咨询服务。