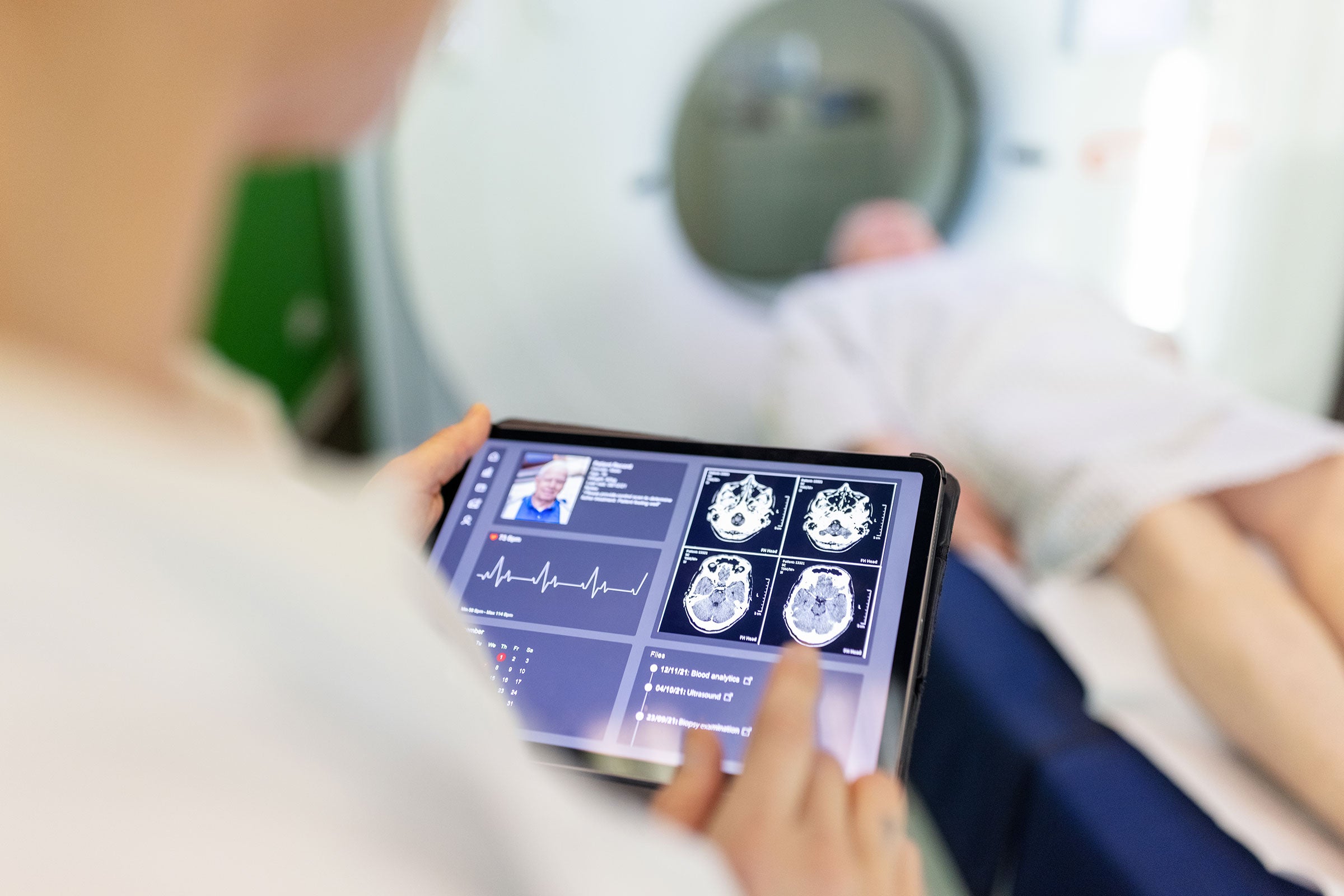
Défis d’accès au marché pour les innovateurs de l’industrie
Les paradigmes de sécurité, de performance et de qualité des produits évoluent à mesure que la technologie médicale progresse, que les appareils deviennent plus interopérables et que les produits de santé numériques prolifèrent. Ces tendances ont élargi le champ d’application de la conformité réglementaire et de la gestion des risques, rendant l’accès au marché plus difficile pour les entreprises du secteur de la santé et des sciences de la vie. Il est essentiel d’adopter des processus de développement de produits qui favorisent l’innovation rapide et qui respectent également les réglementations et les normes mondiales* en matière d’utilisabilité, de sécurité et de conformité.
Prolifération des technologies de santé numériques

Manque de compétences dans le développement de produits centrés sur l’utilisateur

Climat réglementaire complexe
35 %
des adultes américains utilisent des dispositifs de soins de santé portables au moins une fois par jour. (Source)
14 %
d’augmentation des rappels de dispositifs médicaux en 2024, entraînée par des réglementations et une application plus strictes. (Source)
1,77 milliard
de personnes devraient commencer à utiliser des produits de santé numériques d’ici 2029. (Source)
34 %
des rappels de produits médicaux sont dus à de mauvais contrôles de conception. (Source)
Nous aidons les innovateurs de l’industrie à accéder en toute confiance à des marchés hautement réglementés


Réduire le manque de compétences en développement de produits
Assurez un développement de produits conforme grâce à des services de conseil et des logiciels en ingénierie des facteurs humains (HFE)*.
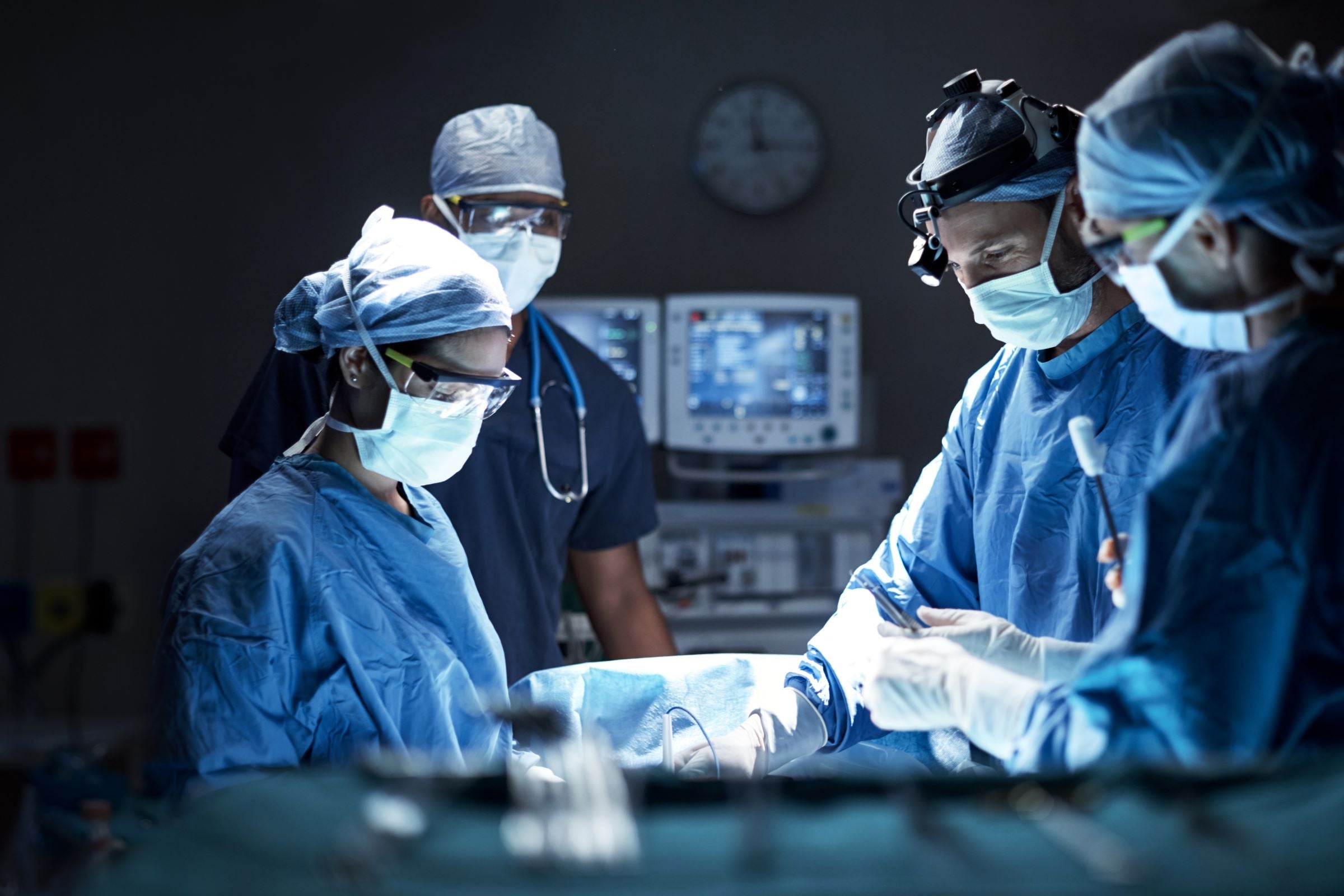
Démontrer la sécurité et vérifier les performances
Respectez les normes du marché, les réglementations et les bonnes pratiques grâce à nos tests et certifications rigoureux.

Automatiser et rationaliser les affaires réglementaires
Facilitez l’accès au marché médical grâce à une expertise réglementaire mondiale et à des logiciels*.
Satisfaire aux exigences en matière d’utilisabilité, de sécurité et de réglementation
Développement de produits et de processus
UL Solutions offre des conseils en ingénierie des facteurs humains et une assistance logicielle pour aider les développeurs de produits et les professionnels de la R&D qui manquent de ressources et de compétences internes à développer des produits médicaux plus sûrs, plus efficaces et plus utilisables*.
Tests et certifications
En tant que leader mondial des sciences de la sécurité, UL Solutions offre des services de test et de certification tiers rigoureux et impartiaux pour aider les entreprises à démontrer leur conformité aux normes de sécurité et de performance des produits et à répondre aux exigences réglementaires mondiales.
Préparation et conformité à la réglementation
Notre réseau d’experts en réglementation aide les clients à accéder au marché dans plus de 20 pays. Nous fournissons des conseils et des logiciels pour automatiser les affaires réglementaires, rationaliser les soumissions de marché et suivre les changements réglementaires*.
Tests et certification pour la santé et les sciences de la vie

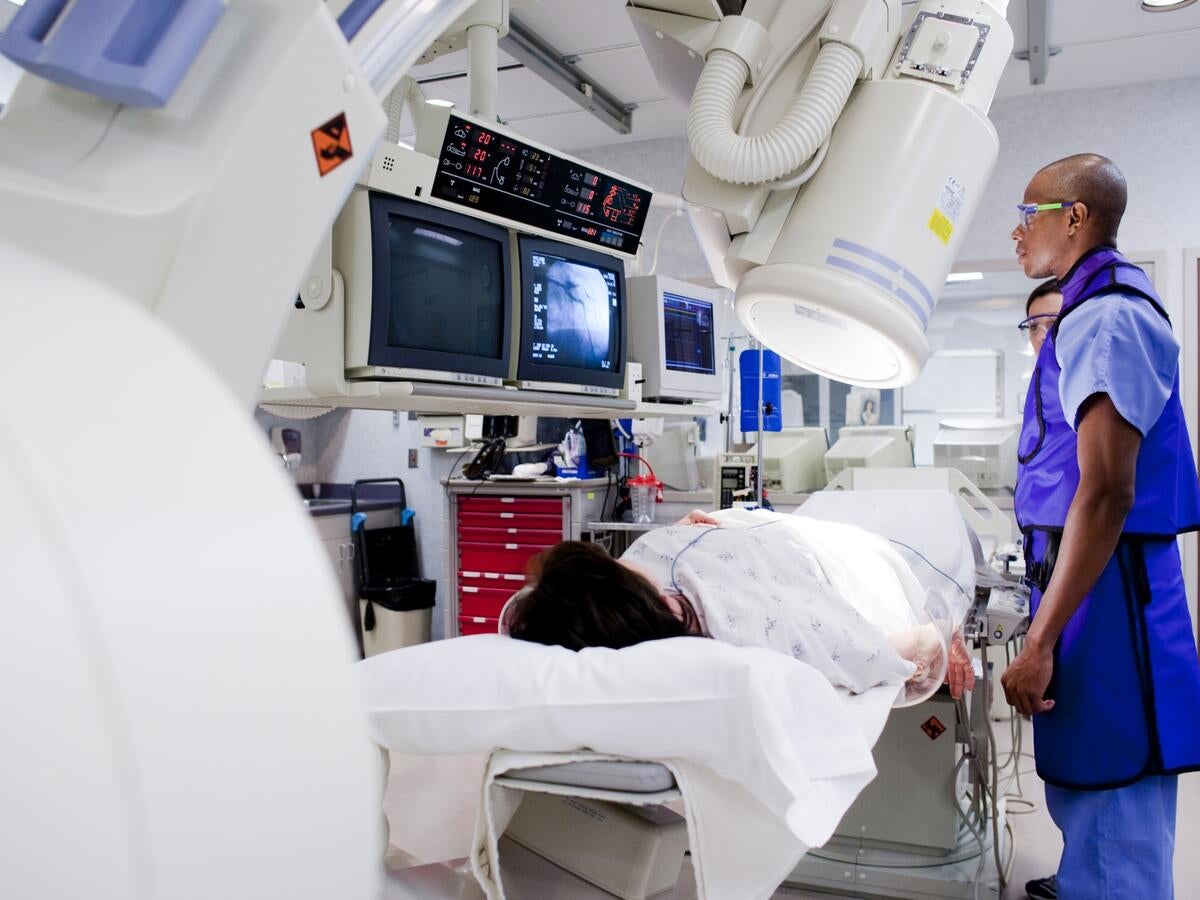
Tests de performance et de sécurité des dispositifs médicaux
Nous effectuons des tests et une certification indépendants et rigoureux des dispositifs médicaux pour aider les fabricants à démontrer les allégations de sécurité et de performance conformément aux exigences réglementaires et aux normes de l’industrie.

Service d’audit des systèmes de gestion de la qualité
Nous fournissons une évaluation indépendante des systèmes de gestion de la qualité des entreprises du secteur de la santé et des sciences de la vie afin de vérifier la conformité à la norme ISO 13485 pour les systèmes de gestion de la qualité des dispositifs médicaux. La certification ISO 13485 est exigée par les régulateurs sur de nombreux marchés.

Certification des logiciels SaMD et de santé
Nous proposons des tests et une certification pour les logiciels en tant que dispositifs médicaux (SaMD) conformément aux normes de l’industrie, notamment CEI 82304-1, CEI 60601-1 partie 14 et CEI 62304, qui peuvent aider à démontrer la sécurité et la qualité du SaMD.
Logiciels et services de conseil pour l’accès au marché médical

Conseil en matière de réglementation et de qualité des dispositifs médicaux et de diagnostic in vitro
L’équipe d’experts en affaires réglementaires d’Emergo by UL aide les sociétés de dispositifs médicaux et de diagnostic in vitro à atteindre leurs objectifs d’accès au marché et à maintenir la conformité après commercialisation dans plus de 20 pays*.

Ingénierie des facteurs humains et conseil en utilisabilité
Notre équipe de Recherche & Conception sur les facteurs humains fournit une assistance en matière d’ingénierie des facteurs humains et d’utilisabilité, notamment des études et analyses utilisateurs, la conception, des tests d’utilisabilité et des formations*.

Suite de gestion des affaires réglementaires (RAMS®)
Emergo by UL propose la plateforme SaaS Regulatory Affairs Management Suite (RAMS) qui permet aux clients d’automatiser les processus d’affaires réglementaires et de tirer parti de nos informations réglementaires sur plusieurs marchés*.
Assurer la sécurité, la conformité et la durabilité pour les innovateurs dans le domaine de la santé et des sciences de la vie
Notre savoir-faire en science de la sécurité et nos logiciels permettent aux innovateurs du secteur de rationaliser l’accès au marché, de gérer les risques liés à la cybersécurité, de constituer une main-d’œuvre conforme, d’améliorer la gestion des risques liés aux fournisseurs et de renforcer les capacités de gestion ESG, les aidant ainsi à développer des produits et des systèmes médicaux plus sûrs et conformes.
Rencontrer nos experts

« Une stratégie réglementaire bien pensée peut faciliter l’innovation, simplifier l’accès au marché et positionner votre entreprise pour une croissance soutenue. »
Evangeline Loh
Directrice principale, Affaires réglementaires & Qualité
« Ensemble, nous créons des solutions qui aident les innovateurs de Medtech à s’assurer que les technologies essentielles atteignent le marché en toute sécurité et efficacement. »
Pamela K. Gwynn
Ingénieure principale, Consommateurs, Technologies de l’information & médicales

Ressource en vedette
Comprendre l’ingénierie des facteurs humains dans les produits médicaux
Notre livre électronique explique comment l’accès aux bonnes pratiques peut aider à guider les principales étapes de l’ingénierie des facteurs humains dans le développement de produits médicaux.
Ressources liées à l’accès au marché

WEBINAIRE À LA DEMANDE
Accès au marché américain pour les dispositifs médicaux : Programme FDA et ASCA 2024
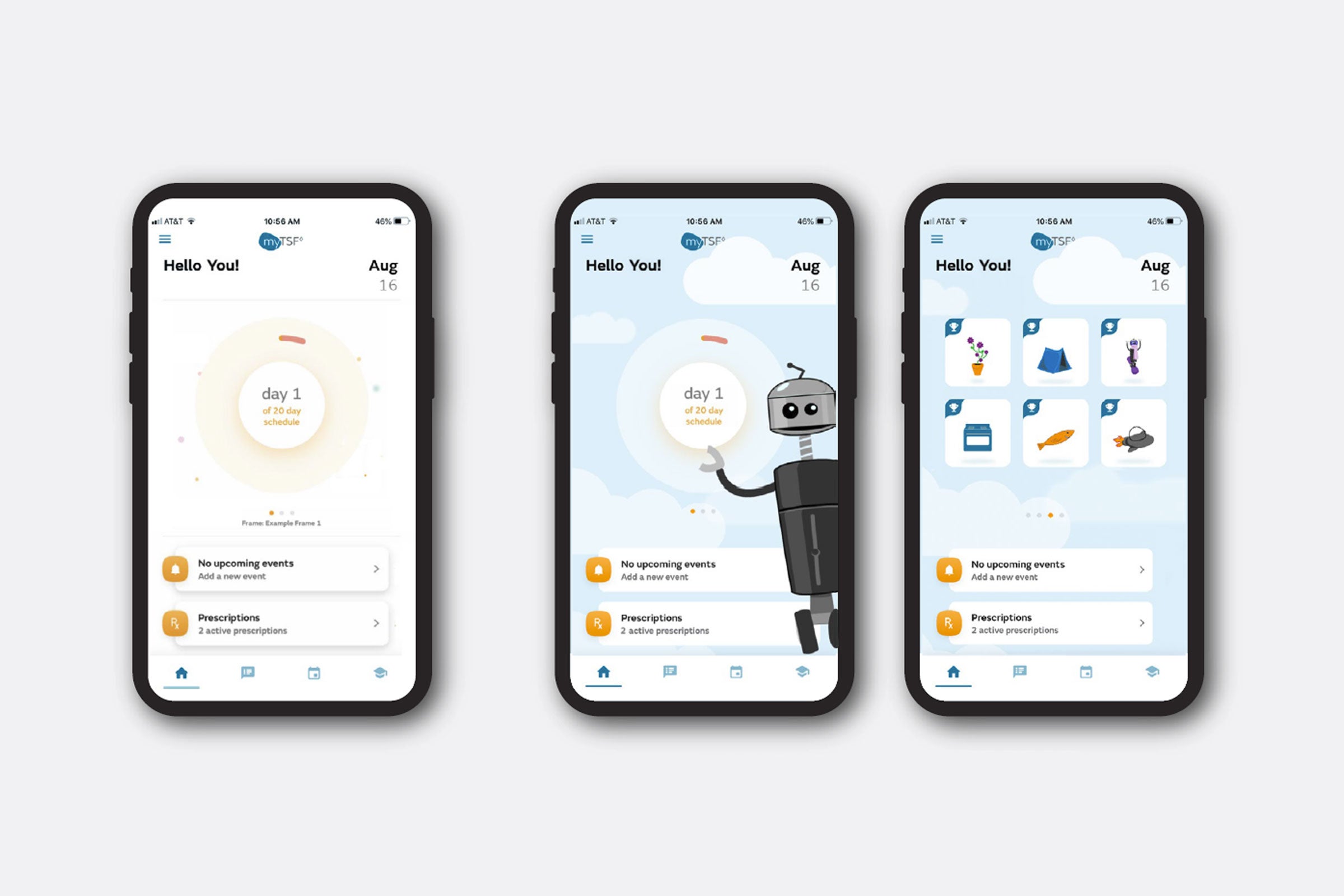
ÉTUDE DE CAS
Révolutionner l’expérience utilisateur avec l’application Smith+Nephew myTSF™
Offres complètes pour le secteur de la santé et des sciences de la vie
* Au sein d’UL Solutions, nous fournissons un large portefeuille d’offres à toutes les industries de dispositifs médicaux. Cela comprend la certification, les services d’organisme agréé/notifié et les services de conseil. Afin de protéger et de prévenir tout conflit d’intérêts et toute perception de conflit d’intérêts, ainsi que de protéger à la fois notre marque et celle de nos clients, nous avons mis en place des processus permettant d’identifier et de gérer tout conflit d’intérêts potentiel et de maintenir notre impartialité. UL Solutions n’est pas en mesure de fournir des services de conseil aux organismes notifiés MDD, MDR, IVDD ou IVDRde l’UE, aux organismes agréés MD de l’UKCA ou aux clients MDSAP.