직원들에게 지속적으로 최신 소식 전달
의료기기 제조업체 및 제약사들에게 끊임없이 변화하는 규제를 따라잡는 것은 고된 작업입니다. 의료 기술은 빠르게 발전하고 있으며, 환자의 안전을 지원하는 규정 준수 시스템의 필요성도 높아지고 있습니다. 귀사 및 귀사의 직원이 최신 미국 Food and Drug Administration(FDA) 규제, GCP(Good Clinical Practice) 교육, HIPAAA 교육, ISO 14971 교육 등을 계속해서 파악하는 데 도움이 될 수 있도록 UL Solutions는 ComplianceWire®를 마련하였습니다.
자동화된 생명과학 학습 관리
UL Solutions의 ULTRUS™ 소프트웨어의 일부인 ComplianceWire 학습 및 자격 관리 시스템은 생명과학 조직을 위해 만들어진 규정 준수 및 자격 관리 교육 학습 관리 시스템(LMS)으로, 업계에서 인정받은 수상 경력의 선도적 솔루션입니다. ComplianceWire는 기본적으로 FDA 21 CFR 11 및 EU Annex 11 전자 기록 검증 요건을 준수합니다. 이 검증된 기술은 미국, 중국, 브라질, 인도 등의 글로벌 규제 기관뿐 아니라, 전 세계 제약, 의료기기, 생물학 기업들이 널리 사용하고 있습니다. ComplianceWire는 생명과학 기업들이 직원을 위한 강력한 자동 교육 기능을 통해 제품의 안전성과 효과성을 유지할 수 있도록 지원합니다.
맞춤형 교육
사용하기 쉬운 콘텐츠 저작 도구인 CourseCreate를 사용하여 ComplianceWire® 교육을 사용자 지정하고, 맞춤형 콘텐츠를 추가하는 방식으로 교육 요구 사항을 해결할 수 있습니다.
21 CFR Part 11 및 EU Annex 11 검증 요건에 부합
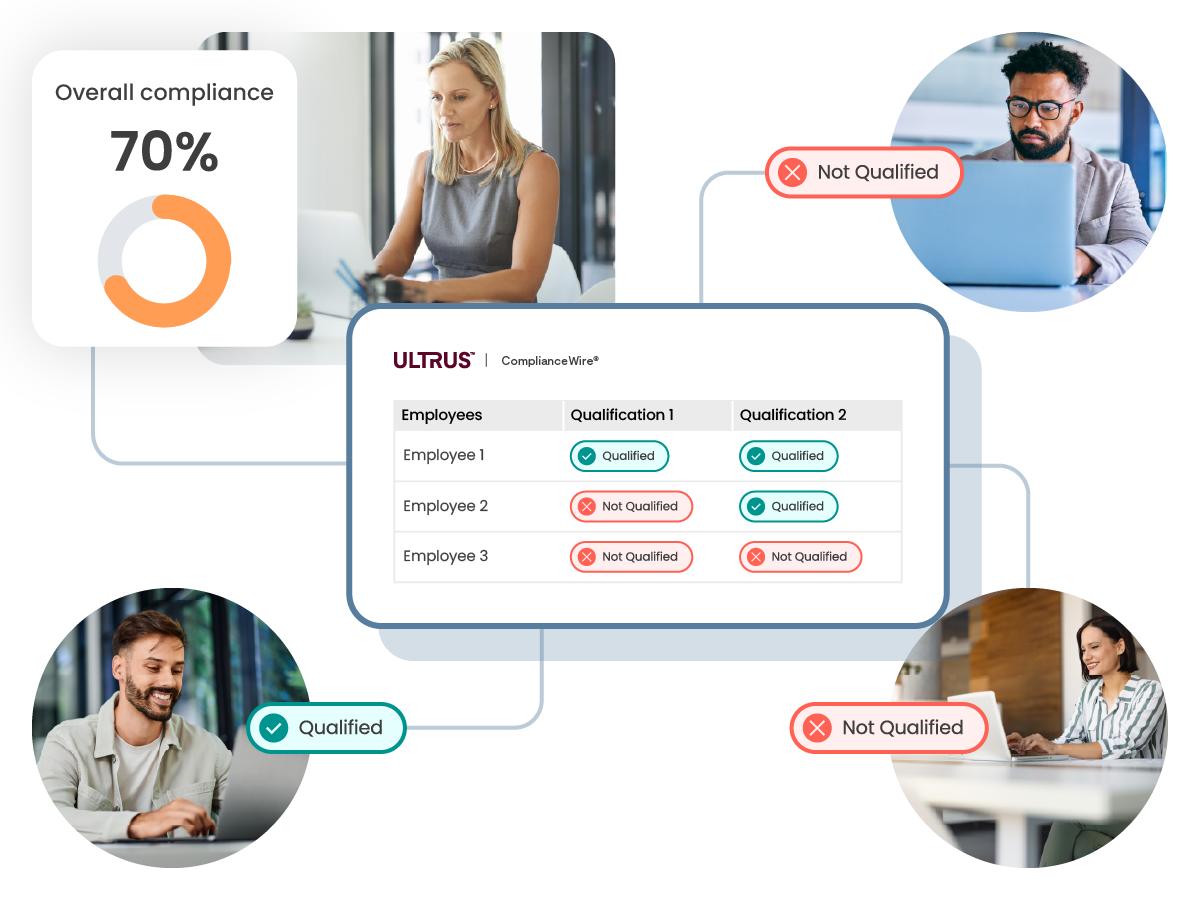
각 구현의 일환으로 고객은 검증 요약 보고서, Part 11 백서, 당사 품질 팀의 감사 및 검증 시험 스크립트를 받습니다. 직무 기능과 같은 기준에 따라 직원들을 교육 집단으로 자동 분류하여 역할 기반 교육 과정을 효과적으로 관리할 수 있습니다. 자동화된 버전 관리는 여러 버전을 수동으로 수행하고 지속적으로 변화하는 SOP 라이브러리를 업데이트할 때 발생하는 사용자 오류의 위험을 감소시킵니다.
e-Learning 라이브러리
1,000개 이상의 이러닝 교육 모듈, 400개 이상의 생명과학 특화 교육 과정, 미국 FDA 및 UL Solutions가 공동 개발한 52개의 과정을 포함한 고품질의 매력적인 지식 및 콘텐츠 자산 라이브러리입니다.
FDA가 사용하는 학습 관리 기술을 신뢰하십시오
UL Solutions 고객은 FDA가 가상 대학에서 검사관 및 조사관을 교육하기 위해 사용하는 것과 동일한 기술 플랫폼 및 과정을 이용할 수 있습니다.
Frequently Asked Questions
- What types of regulated industries typically use ComplianceWire®?
ComplianceWire® is designed for organizations operating in highly regulated environments, particularly within the life sciences. This includes pharmaceutical, biotechnology and medical device clinical organizations, such as contract research organizations (CROs), contract development and manufacturing organizations (CDMOs) and biologics companies, as well as organizations that must comply with Good Practice (GxP) requirements and global regulatory expectations.
- Can ComplianceWire® integrate with other enterprise systems, such as HRIS or document management tools?
Yes. ComplianceWire® is system-agnostic and built to fit easily into the systems your team already uses. The software is designed to integrate with a wide range of enterprise programs, including human resources information systems (HRIS), document management systems, and other learning or business platforms. This compatibility helps streamline user management, training assignments and document distribution across the organization.
- How does ComplianceWire® help organizations prepare for audits or regulatory inspections?
ComplianceWire® supports audit and inspection readiness by maintaining validated electronic records, secure audit trails, detailed training and qualification histories. The system includes standard reports commonly requested by regulatory authorities and enables organizations to quickly demonstrate employee training status, qualifications and compliance with applicable regulations. Because ComplianceWire® is the same learning management system used by the U.S. Food and Drug Administration (FDA) to train its investigators, organizations can produce reports in a format familiar to regulators, helping to streamline audits and inspections.
- Does ComplianceWire® support role‑based or automated training assignments?
Yes. ComplianceWire® enables automated, role‑based training assignments using configurable learner attributes, such as role, department, location or other organizational criteria. As employee roles or attributes change, training assignments can be updated automatically to help maintain ongoing compliance.
- What scalability options does ComplianceWire® offer for growing organizations?
ComplianceWire® is built to scale with organizations as they grow, supporting complex organizational structures, multiple locations and extended enterprise learning for contractors, partners or suppliers. The platform is designed to accommodate increasing numbers of users, training programs and regulatory requirements without compromising performance or compliance oversight.
- What reporting and analytics features does ComplianceWire® include?
ComplianceWire® provides real‑time dashboards and reporting tools that give administrators and managers visibility into training completion, qualification status and compliance gaps. Reports can be used to monitor trends, identify risks, and support internal and external audits, as well as external regulatory inquiries.
- What type of support does UL Solutions provide during the implementation of ComplianceWire®?
UL Solutions has a highly tenured in-house team with deep expertise developed through hundreds of ComplianceWire® implementations and system validations. Because our team understands the system inside and out, they are able to provide responsive, hands-on support from the beginning of the project to the end. The result for our customers is a streamlined implementation process.
생명과학 교육 및 이러닝 기능을 향상시킬 준비가 되셨습니까?
시연을 예약하여 ComplianceWire가 복잡한 규제 요건을 탐색하는 데 어떻게 도움이 될 수 있는지 알아보십시오.